Тол взрывчатое вещество
Тринитротолуол
| Тринитротолуол | |
 |
|
 |
|
| Общие | |
|---|---|
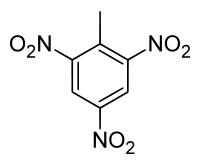
| Систематическое наименование | 2,4,6-тринитрометилбензол |
| Традиционные названия | тротил, тол |
| Химическая формула | C7H5N3O6 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 227,13 г/моль |
| Термические свойства | |
| Температура плавления | 80,85 °C |
| Температура кипения | 295 °C |
| Классификация | |
| Рег. номер CAS | 118-96-7 |
| SMILES | CC1=C(C=C(C=C1[N+](=O)[O-])[N+](=O)[O-])[N+](=O)[O-] =] |
Тринитротолуо́л (троти́л, тол, TNT, 2,4,6-тринитрометилбензол) — одно из наиболее распространённых бризантных взрывчатых веществ. Представляет собой желтоватое кристаллическое вещество с температурой плавления 80,85 °C (плавится в очень горячей воде).
Содержание
Применение
Применяется в промышленности и военном деле как самостоятельно в гранулированном (гранулотол), прессованном или литом виде, так и в составе многих взрывчатых смесей (алюмотол, аммонал, аммонит и другие). В США тротил в промышленности и горном деле не применяют с начала 1990-х годов из-за токсичности продуктов взрыва.
Тротил гораздо стабильнее многих других взрывчатых веществ, например, динамита, к трению и нагреванию, и загорается только при температуре 290 °C, поэтому может быть относительно безопасно нагрет до температуры плавления. Это очень удобно, так как позволяет легко придать нужную форму при помощи литья. Литой или прессованный тротил можно поджечь. Он горит без взрыва желтоватым пламенем. Для взрыва обычно необходимо использование детонатора, однако порошкообразный тротил с примесями может иметь повышенную чувствительность к внешним воздействиям, в том числе и к пламени.
Несмотря на стабильность тринитротолуола, во многих применениях и его стараются заменить на ещё более стабильные взрывчатые вещества. Например, Вооруженные силы США планирует заменить тротил в крупнокалиберных снарядах на вещество IMX-101.
Тринитротолуол был получен в 1863 году немецким химиком Юлиусом Вильбрандом.
Обладает свойствами антимикотика, ранее применялся в медицине в составе противогрибковых препаратов «Ликватол» и «Унгветол», но из-за токсичности и появления более эффективных лекарственных средств практически вышел из медицинского употребления.
Получение
Первый этап: нитрование толуола смесью азотной и серной кислот. Серная кислота используется как водоотнимающий агент.
Второй этап: затем смесь моно- и динитротолуола нитруют в смеси азотной кислоты и олеума. Олеум используется как водоотнимающий агент.
Излишек кислоты от второго этапа можно использовать для первого.
Тринитротолуол

На фото — кристаллический препарат тринитротолуола (2,4,6-тринитротолуол, C7H5N3O6). Тринитротолуол, или ТНТ, или тротил, входит в первую десятку органических веществ, название которых легко вспоминает человек, далекий от химии. В начале ХХ века он интенсивно использовался в качестве бризантного взрывчатого вещества военного и промышленного назначения. Тринитротолуол-тротил до сих пор служит эквивалентом для оценки количества энергии, выделяемой при ядерных взрывах, подрывах химических взрывчатых устройств, падениях астероидов и комет, взрывах вулканов.

При комнатной температуре тринитротолуол представляет собой желтое кристаллическое вещество. Впервые он был получен в 1863 году немецким химиком Юлиусом Вильбрандом (на многих интернет-ресурсах этот синтез и открытие тринитротолуола ошибочно приписывают его отцу — немецкому врачу и судебному медику Йозефу Вильбранду). Тринитротолуол получают, обрабатывая толуол азотной кислотой в присутствии концентрированной серной кислоты и олеума — раствора SO3 в серной кислоте. Обработка толуола азотной кислотой — нитрование — происходит постадийно, на каждой стадии в молекулу вводится одна нитрогруппа (–NO2), и если динитротолуол еще можно получить, используя в качестве катализатора концентрированную серную кислоту, то для введения третьей группы –NO2 необходим более активный катализатор — олеум. После нитрования кристаллы тринитротолуола отмывают водой от загрязнений и высушивают.
Непосредственно после первого успешного синтеза тринитротолуола его потенциал как нового взрывчатого вещества не был раскрыт. До 1890-х годов тринитротолуол, получаемый в скромных количествах, использовали только в качестве желтого красителя для текстиля. Исследователи не смогли разглядеть в нем взрывчатое вещество три десятка лет из-за того, что это соединение не так легко детонирует. По сравнению с основными взрывчатыми веществами, которые в те времена рассматривались как замена дымному пороху, — тринитроглицерином или нитроцеллюлозой — тринитротолуол считался исключительно устойчивым, да и мощность его взрыва меньше, чем у нитроцеллюлозы и нитроглицерина. Разглядеть в тринитротолуоле потенциальную взрывчатку удалось только в 1891 году другому немецкому химику — Карлу Хойссерманну (Karl Häussermann).
Стать «эталонным» взрывчатым веществом тринитротолуолу помогли относительная простота и дешевизна его промышленного получения, безопасность при хранении, транспортировке и легкость снаряжения им боеприпасов. Тротил можно расплавить, заполнить его расплавом любую емкость или придать обусловленную тем или иным применением форму. Такое возможно из-за того, что температура плавления тринитротолуола составляет 80°С, а температура разложения — 240°С, поэтому в отсутствие искр или источников открытого огня работа с расплавленным тротилом практически безопасна, чего нельзя сказать про работу с нитроглицерином или нитроцеллюлозой.

Плавление 2,4,4-тринитротолуола. Фото с сайта creationwiki.org
С 1890-х годов тринитротолуол стал использоваться как взрывчатое вещество гражданского назначения. Из него изготавливали тротиловые шашки для горных работ, расчистки ландшафта при прокладке железных и автодорог, сносе зданий. Снаряжение артиллерийских боеприпасов, мин и бомб тротилом началось в 1902 году, первыми были немцы, в 1907 году технологию производства тротиловых боеприпасов освоили британцы. Первое полномасштабное применение произошло во время Первой Мировой войны. Практика показала, что тринитротолуол оказался более удобным для ведения боевых действий, чем его основной конкурент того времени — пикриновая кислота (см. тринитрофенол). Боеприпасы с пикриновой кислотой, в отличие от снарядов с тринитротолуолом, могли самопроизвольно взрываться от удара. Это происходило из-за того, что пикриновая кислота могла реагировать с металлами, из которых изготавливали артиллерийские гильзы, образуя при этом взрывоопасные соли — пикраты. Также пикриновая кислота относительно хорошо растворяется в воде (при 20°С в 1 литре воды растворяется уже 12,7 г кислоты), а значит, она могла поглощать воду из влажного воздуха, теряя при этом взрывчатую способность. С тринитротолуолом такого не происходит: он плохо растворяется в воде (при 20°С в 1 литре воды растворяется всего 0,13 г вещества).
При взрыве тринитротолуол разлагается в соответствии со следующим уравнением:
Если посчитать объем выделяющихся при взрыве тротила газов, даже занижая оценку (то есть приводя его к комнатной температуре и считая в этих условиях газами только азот и угарный газ), то объем продуктов детонации будет примерно в 800 раз больше объема самого тринитротолуола. Уже такая оценка говорит о тротиле как о мощном взрывчатом веществе (взрыв — химическая реакция, сопровождающаяся в том числе и значительным изменением объема). При взрыве тринитротолуола значительно увеличивается температура, при этом выделяющаяся при его разложении вода будет газообразной, а продукты взрыва займут больший объем, чем при комнатной температуре. Поэтому на самом деле объем продуктов разложения будет в тысячи раз превосходить объем самого взрывчатого вещества. Резкое увеличение объема и определяет мощность взрывчатки. Точно рассчитать или измерить энергию взрыва образца тринитротолуола невозможно: эту величину можно знать, только зная температуру взрыва, а она, в свою очередь, зависит от типа взрыва — при детонации в замкнутом объеме температура выше, чем в открытом. Для стандартизации принято считать, что при взрыве килограмма тротила выделяется 4,2×10 3 килоджоулей, одна килотонна в тротиловом эквиваленте соответствует при этом 4,2×10 6 мегаджоулям энергии.
Хотя основное применение тринитротолуола — снаряжение боеприпасов, не нужно забывать, что он использутся и в мирных целях: при строительстве туннелей, для сноса старых зданий и расчистки земли под реновацию инфраструктуры городов. Из тринитротолуола получают 1,3,5-тринитробензол и 1,3-динитробензол, которые тоже являются взрывчатыми веществами, но, в отличие от тротила, используются не самостоятельно, а в композициях с нитроцеллюлозой при изготовлении бездымного пороха. Тринитротолуол считается канцерогеном и веществом, вызывающим анемию и поражение печени. Также он оказывает раздражающее действие на кожу, окрашивая ее в желтый или оранжевый цвет, так что совсем уж безопасной работу с тринитротолуолом назвать нельзя.
История создания, описание, свойства тротила
С середины ХIX многие ученые проводили эксперименты по синтезированию и созданию новых видов взрывчатых веществ, которые бы могли по мощности превзойти пороховые заряды. И только в 1863 году немецкому ученому Юлиусу Вильбрандому удалось синтезировать первый образец тротила.
 Тротиловая шашка, фото
Тротиловая шашка, фото
История создания тротила
| Дата | Событие |
| 1863 г. | Создание немецким ученым Юлиусом Вильбрандом первого образца тротила |
| 1891 г. | Первое массовое изготовление и использование в Германии |
| 1905 г. | Начало экспериментов по созданию тротила в США и последующее производство |
| 1909 г. | Изготовление тротила в России и других странах |
Изготовление данного взрывчатого вещества началось только в 1891 году в Германии, под руководством известного немецкого химика Генриха Каста. Изготовление и испытания проводились под грифом «Секретно», где в последующем было присуждено название — тротил.
В 1905 году в Германии была изготовлена первая крупная партия, имеющая вес более ста тон. В этом же году состав тротила был раскрыт американскими учеными, которые начали работу по производству взрывчатки в США. Далее секрет был открыт всему миру, после чего началось производство в России и других странах мира.
 Тротиловая ручная граната времен Первой мировой войны
Тротиловая ручная граната времен Первой мировой войны
К началу Первой мировой войны было изготовлено большое количество тротила, который активно использовался всеми странами. Работы по созданию совершенного состава взрывчатого вещества продолжались вплоть до 1940 года, после чего была утверждена окончательная формула тротила.
Самое массовое изготовление взрывчатого вещества было зафиксировано в США в 1945 году , когда на военные и промышленные нужды было изготовлено более 1 млн тон.
Особенности использования
Тротил является взрывчатым веществом с большой мощностью, и имеет множество достоинств, которые выделяют его от других веществ. Тротил может находиться в нескольких формах:
- гранулированная;
- прессованная;
- литая.
Все это позволяет использовать его не только в военном деле, но и в промышленности, например, в горной. Также тротил обладает высоким уровнем безопасности на всех этапах использования и большим сроком хранения без потери всех взрывчатых свойств, который составляет до 20 лет.
 Применение тротила в подрыве боеприпасов
Применение тротила в подрыве боеприпасов
Часто используют тротил в соединениях с другими взрывчатыми веществами, что позволяет улучшить качество, снизить чувствительность и добиться постоянного состояния других веществ.
Основное применение тротила:
- военное дело;
- промышленность;
- медицина.
Ранее тротил активно применялся в медицине, и он входил в состав некоторых медицинских препаратов. Сейчас он входит в состав антигрибковых средств. Также ученые всего мира продолжают работы по созданию взрывчатого вещества, превосходящего мощность, стабильность и другие свойства тротила.
Физические и химические свойства тротила
Тротил получают с помощью нитрования такого вещества, как тол. Всего существует шесть изомеров, которые имеют одну и ту же формулу, но разно положение относительно бензольного ядра, что приводит к различным химическим свойствам.
Основные химические свойства тротила:
| температура затвердевания | 85°С |
| температура плавления | 82°С |
| температура кипения | 295°С |
| теплота плавления | 21,41 ккал/г |
| теплота кристаллизации | 5,6 ккал/моль |
| гигроскопичность | 0,05% |
| растворимость — при температуре воды 25°С/100°С | 0,02/0,15 |
Основные физические свойства тротила:
| состояние | твердое |
| скорость детонации (при плотности тротила 1,64 кг/м 3 ) | 6,95 сек. |
| дробящее воздействие по Гессу | 16 мм |
| дробящее воздействие по Касту | 3,9 мм |
| объем газообразования при детонации | 730 л/кг |
| фугасность | 285 мл |
| чувствительность при падении (10 кг тротила с высоты 25 см) | до 8% детонации |
| максимальный срок хранения | 25 лет, после чего возрастает чувствительность к детонации |
Плотность тротила
Плотностью является соотношение массы тела к занимаемому объему. Плотность взрывчатого вещества составляет 1654 кг/м3.
Мощность
Мощность взрыва тротила измеряется в тротиловом эквиваленте. При взрыве тротила выделяется энергия, которая составляется 4184 Джоулей или 1000 термохимических калорий на 1 грамм тротила.
Теплота взрыва
Теплотой взрыва тротила называется объем энергии, выделяемый при взрывчатом вращении. При взрыве 1 кг тротила она составляет от 4100 до 4700 кДж.
Дробящее воздействие
Дробящее воздействие (бризантность) является одной из характеристик взрывчатых веществ, которая определяет способность вещества на послевзрывное воздействие в окружающей среде. Бризантность тротила составляет в 16,5 мм, что на порядок выше других веществ, таких как гексоген (4,2 мм) и октоген (5,4 мм).
Тротиловый эквивалент
Тротиловым эквивалентом называется мера энерговыделения при взрыве взрывчатых веществ и определяющая количество исходящей энергии. Данная мера используется для вычислений мощности взрыва, и составляет 4184 Дж на 1000 кал/г.
 Взрыв тротилового заряда весом в 100 кг
Взрыв тротилового заряда весом в 100 кг
В тротиловом эквиваленте проходит измерение и сравнение мощности взрывчатых веществ в соотношении с тротилом.
| Название взрывчатого вещества | Мощность |
| тротил | 1,0 |
| тринитрорезорцинат свинца (ТНРС) | 0,39 |
| порох | 0,55 -0,66 |
| тетрил (мощнее тротила) | 1,25 |
| гексоген | 1,6 |
| тритонал | 1,6 |
| Этиленгликольдинитрат (ЭГДН) | 1,6 |
| Октоген | 1,7 |
Изготовление тротила
Взрывчатка является твердым веществом с высокой температурой плавления, технология производства тротила достаточно сложна. Всего существует два способа его получения:
- одностадийный;
- двухстадийный.
Одностадийный способ включает в себя такие процессы:
- сушка при температуре 100°С;
- измельчение и просеивание;
- получение вещества и промывка;
- кристаллизация;
- сушка при температуре 100°С;
- просеивание;
- укупорка.
Во время изготовления тратила первым этапом является сушка, последующее измельчение и просеивание вещества. Далее идет смешивание с нитротором, азотной кислотой и пентаэритритом. Смешивание происходит с определенной скоростью, которая не позволяет подняться температуре веществ до 20°С.
 Тротил. Фото
Тротил. Фото
После сушки вещество принимает кристаллический вид. Полученные кристаллы проходят дополнительную сушку, просеивание и отжимание. Последним процессом в изготовлении тротила является укупорка с использованием спирта.
Двухстадийный способ включает в себя:
- получение сернокислотного эфира;
- смешивание дополнительных веществ с одновременной сушкой при температуре до 60°С.
Данный способ изготовления тротила появился первым и использовался по причинам простоты и перспективности. Во время смешивания и сушки добавлялась азотная кислота, пантаэритрит и серная кислота. Все эти вещества смешивались поэтапно при различной температуре нагревания.
Взрывчатые вещества нормальной мощности
Тротил (тринитротолуол, тол, ТНТ) – основное бризантное ВВ, применяемое для подрывных работ и снаряжения большинства боеприпасов; он представляет собой кристаллическое вещество от светло-желтого до светло-коричневого цвета, горьковатое на вкус. Тротил негигроскопичен и практически нерастворим в воде; удельный вес – 1,66. В производстве тротил получается в виде порошка и в виде мелких чешуек (чешуйчатый тротил). Он хорошо прессуется до объемного веса 1,60.
Тротил плавится без разложения при температуре около 81°С; объемный вес затвердевшего после плавления (литого) тротила – 1,55-1,60; температура вспышки – около 310°С; на откры том воздухе тротил горит желтым, сильно коптящим пламенем без взрыва. Горение тротила в замкнутом пространстве может переходить в детонацию.
К удару, трению и тепловому воздействию тротил малочувствителен, что является большим его достоинством. Прессованный и литой тротил от улара обычной ружейной пули нс взрывается и нс загорается. С металлами тротил химически не взаимодействует.
Восприимчивость тротила к детонации зависит от его состояния. Прессованный и порошкообразный тротил безотказно детонирует от капсюля-детонатора № 8 (штатный тин), литой же и чешуйчатый тротил детонирует от промежуточного детонатора из прессованного тротила или из другого бризантного ВВ повышенной или нормальной мощности.
Химическая стойкость тротила весьма высока; длительное нагревание при температуре до 130°С мало изменяет его взрывчатые свойства, он не теряет этих свойств и после длительного пребывания в воде. Под влиянием солнечного света тротил претерпевает физико-химические превращения, сопровождающиеся изменением его цвета и некоторым повышением чувствительности к внешним воздействиям.
Тротил образуется в результате обработки толуола (жидкий продукт коксохимической и нефтеперерабатывающей промышленности) смесью азотной и серной кислот. Порошкообразный тротил получается путем его кристаллизации из растворителей. Чешуйчатый тротил получают путем снятия (бронзовыми ножами) тонкой пленки литого тротила после застывания его на специальных барабанах.
Из тротила прессованием или заливкой изготовляются различные заряды и подрывные шашки.
Для снаряжения боеприпасов тротил применяется не только в чистом виде, но и в сплавах с другими ВВ (гексогеном, тетрилом и др.). Чешуйчатый тротил входит в состав некоторых ВВ пониженной мощности (например, аммонитов).
Для производства подрывных работ тротил, как правило, применяется в виде прессованных подрывных шашек (рис. 4.5):
- • больших – размерами 50 × 50 × 100 мм и весом 400 г;
- • малых – размерами 25 × 50 × 100 мм и весом 200 г;
- • буровых (цилиндрических) – высотой 70 мм, диаметром 30 мм и весом 75 г.

Рис. 4.5. Тротиловые подрывные шашки:
а – большая; б – малая; в – буровая: 1 – запальные гнезда
Все подрывные шашки имеют запальные гнезда для капсюля-детонатора № 8. Для более надежного сочленения со средствами взрывания запальные гнезда некоторых шашек делаются с резьбой. Для защиты шашек от внешних воздействий их покрывают слоем парафина и обертывают бумагой, на которую затем наносится еще один слой парафина.
Подрывные шашки с целью обеспечения удобств их хранения и перевозки упаковываются в деревянные ящики: большие шашки – по 62 шт. с добавлением одной малой шашки (вес ВВ в ящике – 25 кг); малые шашки – по 123 шт. с добавлением одной большой шашки (вес ВВ в ящике – 25 кг); буровые шашки – по 250 шт. без добавления шашек другого типа (вес ВВ в ящике – 18,75 кг).
Комплектование отдельных ящиков подрывными шашками с запальными гнездами с резьбой производится по одному из следующих вариантов:
- • все шашки в ящике имеют гнезда с резьбой; этот вариант может применяться в отношении всех трех типов шашек;
- • во всем ящике только одна шашка имеет гнездо с резьбой, гнезда остальных шашек гладкие; данный вариант может применяться в отношении только больших и малых шашек;
- • в ящике нет ни одной шашки с гнездом с резьбой; по такому варианту могут упаковываться только буровые шашки.
В каждом ящике больших и малых шашек шашка с запальным гнездом с резьбой (при упаковке по первому варианту – любая из шашек) укладывается в верхнем ряду под съемной планкой и обращается гнездом наружу.
Пикриновая кислота (тринитрофенол, мелинит) представляет собой кристаллическое вещество желтого цвета с удельным весом 1,81. Пикриновая кислота имеет горький вкус, пыль ее сильно раздражает дыхательные пути.
Пикриновая кислота в холодной воде растворяется слабо, в горячей – несколько лучше. Растворы пикриновой кислоты сильно окрашивают кожу и ткани в желтый цвет.
Пикриновая кислота хорошо прессуется; плавление ее происходит при температуре 122,5°С без разложения. Объемный пес прессованной и литой пикриновой кислоты – приблизительно 1,60.
Чувствительность пикриновой кислоты к удару, трению и тепловому воздействию несколько выше чувствительности тротила; от прострела ружейной пулей она может взрываться. Температура вспышки пикриновой кислоты – около 300°С; горит сильно коптящим пламенем, но несколько энергичнее, чем тротил. Горение небольшого количества пикриновой кислоты на открытом воздухе в детонацию не переходит; горение ее в количестве, превышающем 200 кг, может переходить в детонацию. Сжигание даже незначительного количества пикриновой кислоты в замкнутом пространстве может привести к детонации.
Пикриновая кислота но сравнению с тротилом обладает несколько лучшей восприимчивостью к детонации. Порошкообразная и прессованная пикриновая кислота взрывается от капсюля-детонатора № 8. Литая пикриновая кислота от капсюля-детонатора № 8 детонирует не всегда; поэтому для взрыва литой пикриновой кислоты требуется применять промежуточный детонатор.
Пикриновая кислота – вещество химически стойкое, но весьма активное; она химически взаимодействует с металлами (за исключением олова), образуя соли, называемые пикратами.
Пикраты представляют собой взрывчатые вещества, в большинстве случаев более чувствительные к механическим воздействиям, чем сама пикриновая кислота. Особенно чувствительными являются пикраты железа и свинца.
Пикриновая кислота получается путем обработки фенола (продукт, получаемый из каменноугольного дегтя или из бензола) смесью азотной и серной кислот. Она применяется как в чистом виде, так и в виде различных сплавов с динитронафталином для снаряжения некоторых боеприпасов.
Пластичное ВВ (пластит-4) представляет собой однородную тестообразную массу светло-кремового цвета, объемный вес – 1,4. Пластит изготовляется из порошкообразного гексогена (80%) и специального пластификатора (20%) путем тщательного их перемешивания.
Пластит-4 негигроскопичен и нерастворим в воде; легко деформируется усилием рук. Легкая деформируемость позволяет использовать пластит для изготовления зарядов требуемой формы на месте производства подрывных работ.
Пластические свойства пластита-4 сохраняются при температуре от -30 до +50°С. При отрицательных температурах пластичность его несколько снижается; при температурах выше +25°С пластит-4 размягчается и прочность изготовленных из него зарядов уменьшается.
К удару, трению и тепловым воздействиям пластит-4 малочувствителен (его чувствительность лишь немного выше чувствительности тротила). При простреле ружейной пулей, как правило, не взрывается и не загорается; при зажигании горит; горение его в небольшом количестве (до 50 кг) протекает энергично, но без взрыва. С металлами пластит-4 химически не взаимодействует. Детонирует он от капсюля-детонатора № 8, погруженного в массу заряда на глубину не меньше 10 мм.
Пластит-4 не обладает свойствами липкого вещества, поэтому при производстве подрывных работ необходимо предусматривать соответствующее крепление пластитовых зарядов к подрываемым объектам.
Три в одном: тротил, пластит и динамит и их история
![]()

Динамит
В 1847 году итальянский химик Асканио Собреро синтезировал жидкость, позволявшую «левитировать» тяжёлые предметы. В миру она получила название «нитроглицерин». Но Собреро и не подозревал, какие серьёзные последствия его открытие будет иметь для всего мира.
Полученная жидкость взрывалась практически от всего: от нагрева, удара или трения. Неправильное хранение тоже приводило к взрыву.
После синтеза вещество лучше было сразу пускать в дело. А дел было много. На повестке дня стояло промышленное развитие: человечеству требовались руда, тоннели, дороги, котлованы, так что волшебная жидкость пришлась очень к месту. И как было бы замечательно, если бы так всё и осталось, — но увы, увы…
По легенде, однажды, когда Альфред Нобель перевозил нитроглицерин, некоторое его количество вылилось из бутылки и впиталось в землю — ею, за неимением пупырчатой плёнки, обкладывали бутылки в телеге. Поэкспериментировав с полученной грязью, знаменитый изобретатель и филантроп обнаружил, что по мощности взрыва получившаяся смесь практически не уступает нитроглицерину, и при этом её можно хранить, кидать, резать, перевозить — да хоть горшки лепить, лишь бы в печь не сажать.
Сам Нобель эту байку яростно отрицал — дескать, чтобы у меня, да что-то пролилось!
Если бы он так небрежно относился к нитроглицерину, то вместо премии Нобеля у нас сейчас была бы исключительно премия Дарвина.
Но невозможно вытравить из народного сознания то, что имеет глубокую психологическую основу — страх.
Нобель был успешным предпринимателем, наладившим в Швеции, а затем и за рубежом производство нитроглицерина. Его заказчиками становились как правительства, так и частные лица. Но успешным он оказался только касательно доходов. А вот по части инцидентов удачливым его не назовешь…
У Альфреда взрывалось всё: заводы, корабли, лаборатории. Во время одного из взрывов погиб его младший брат. Люди боялись внеплановых детонаций, государства издавали законы о запрете производства нитроглицерина на своей территории.
Поэтому в сознании обывателя Нобель был кем-то вроде Бафомета — страшного сатанинского идола.
Впрочем, сам изобретатель настаивал, что целенаправленно экспериментировал с 1864 года с пропиткой разнообразных веществ нитроглицерином. В качестве одного из них использовалась кремнистая земля — кизельгур, и это был успех. Так путём долгого труда в 1866 году Альфред Нобель изобрёл динамит.

Принцип самой знаменитой на планете взрывчатки прост: берём вещество-поглотитель, пропитываем его нитроглицерином, вставляем капсюль — и вуаля.
Изобретение приняли на ура. Одним из его вариантов стали так называемые желатин-динамиты, более известные как «гремучие студни». Благодаря тому, что синтезировать нитроглицерин и нитроцеллюлозу было сравнительно несложно, русские революционеры-народники стали активно использовать это сочетание для производства своих бомб — химиками они были хорошими.
Так, гремучим студнем собственного производства товарищ Кибальчич отправил к праотцам императора Александра II (чем на практике продемонстрировал невозможность уничтожить монархию путём убийства монархов).
Но всё это уже давняя история.
Тротил
Пока Нобель возился с детонаторами и поглотителями, в 1863 году химик Вильбранд в Германии синтезировал то, что ни один человек, будучи навеселе, не выговорит: тринитротолуол. Может быть, поэтому у него хватает альтернативных названий: тротил, TNT, тол.
Он был мощнее тогдашних пороховых смесей и слабее нитроглицерина, однако, в отличие от последнего, не взрывался от любой встряски. В то же время производить его на коленке оказалось очень непросто. Причём настолько, что отлаженный способ промышленного производства для нужд армии и флота придумали в Германии только в 1891 году.
Зато преимуществ у новой взрывчатки из тринитротолуола было просто море. Она легко плавилась, но не взрывалась, поэтому тол можно было безопасно заливать в снаряды в качестве боевого вещества. На его базе разработали большое количество взрывчатых веществ, которые активно применялись и на полях сражений, и во взрывном деле.
Одним из таких производных стал аммонал. В быту он показал себя лучше динамита и широко использовался — в частности, при строительстве каналов в сталинском СССР, сокращая усилия по маханию кайлом и лопатой.
При этом на войне его применяли весьма ограниченно: аммонал годился для мин и гранат, но не подходил для снарядов, поскольку взрывался при выстреле орудия.
Но в целом на войне тринитротолуол и взрывчатые вещества на его основе зарекомендовали себя весьма впечатляюще. На протяжении ХХ века снаряды и бомбы, снаряжённые им и его апгрейдами, активно сыпались на голову человечества, знаменуя торжество прогресса.
К концу ХХ века тол стал самым массовым взрывчатым веществом.
Пластит
в 1890-х годах немецкие военные впервые синтезировали гексоген. Но официально считается, что его открыл в 1898 году немецкий химик Геннинг.
Поначалу гексоген пытались использовать в качестве лекарства, поскольку его химическая формула похожа на уротропин — препарат, который используют до сих пор.
Только через 20 лет выяснилось, что это мощнейшее взрывчатое вещество. С 1920 года его начали производить для военных целей.
Сейчас гексоген ассоциируется главным образом с исламскими террористами, но на самом деле его активно использовали уже во Второй мировой войне. К примеру, смесь гексогена с тринитротолуолом и алюминиевой пудрой получила название «Торпекс». Ей начиняли так называемые «прыгающие бомбы» Барнса Уоллеса, сброшенные с самолетов на дамбы в долине реки Эдер и Мёне в 1943 году. Бомбы, как «блинчики», скакали по воде, чтобы приблизиться к плотине, защищённой сетями.
В результате операции, получившей название «Порка», долину Рура затопило.
Пластит — так именуются пластичные взрывчатые вещества — соотносится с гексогеном примерно так же, как динамит с нитроглицерином. Гексоген входит в пластичную взрывчатку в качестве основы. Гибкость пластификатора позволяет без проблем лепить из него шарики, куличики, запихивать в щели, окружать им опоры, устраивать направленные взрывы и всё такое.
Пластит дороже в производстве, чем гексоген, зато гораздо удобнее в применении. В мире существует масса разновидностей пластической взрывчатки — в частности, знаменитая американская C-4.
В настоящее время это самая популярная взрывчатка — однако сложно сказать, надолго ли. Ведь прогресс не стоит на месте. Каждый год синтезируется новое взрывчатое вещество — более мощное, более надёжное и более разрушительное. Человечество жаждет, чтобы было как можно «круче» и «страшнее».